AI辅助糖尿病药物开发,效果提升3倍,中国团队研究登Nature子刊
有望成为长效药
明敏 发自 凹非寺
量子位 | 公众号 QbitAI
AI辅助制药,找到传统方法难以发现的关键盐桥,激动剂活性直接提升2-3倍!
一项来自中国团队的研究,登上Nature子刊Scientific Report。

它研制出的双靶点激动剂可被应用于治疗二型糖尿病和肥胖症。
不仅活性更高,而且在血浆中的半衰期也更长,即可作用更长时间。
该激动剂已在小鼠和猕猴身上进行实验,验证其具有治疗二型糖尿病和肥胖症的潜力。
而能够发现这一关键盐桥,AI在其中功不可没。
用AI模拟生物机制
GLP-1R(胰高糖素样肽-1受体)和GIPR(依赖葡萄糖的胰岛素促进多肽受体)是治疗二型糖尿病和肥胖症的“明星靶点”。
被炒得沸沸扬扬的司美格鲁肽(Semaglutide),正是一种GLP-1R激动类药物。
不过司美格鲁肽上市后暴露出了比较严重的副作用,比如导致肌肉含量下降、出现基础代谢问题、肠道副作用等,甚至长期服用还可能导致抑郁。
这意味着,该领域还有非常大的探索价值和提升空间,治疗药物还需要不断迭代。
本项研究正是出于这一目的进行。
以往研究表明,替尔泊肽(Tirzepatide)是一种已显示出在血糖和体重控制方面优于选择性GLP-1R激动剂的双重激动剂肽。
它具有临床效果,但是其结构基础和部分激动活性仍有待进一步研究。
本项研究使用分子动力学模拟,发现非乙酰化Tirzepatide与GLP-1R/GIPR在K20位点形成的关键盐桥能够起到稳定靶点激活态构象的作用,这一特征在冷冻电镜结构中未被观察到。
而Tirzepatide在K20位点引入的酰化侧链则会破坏这一盐桥作用,造成酰化修饰后的Tirzepatide激动活性下降。
基于这些发现,团队开发了一种优化策略,通过重新定位乙酰化侧链来增强激动剂活性。
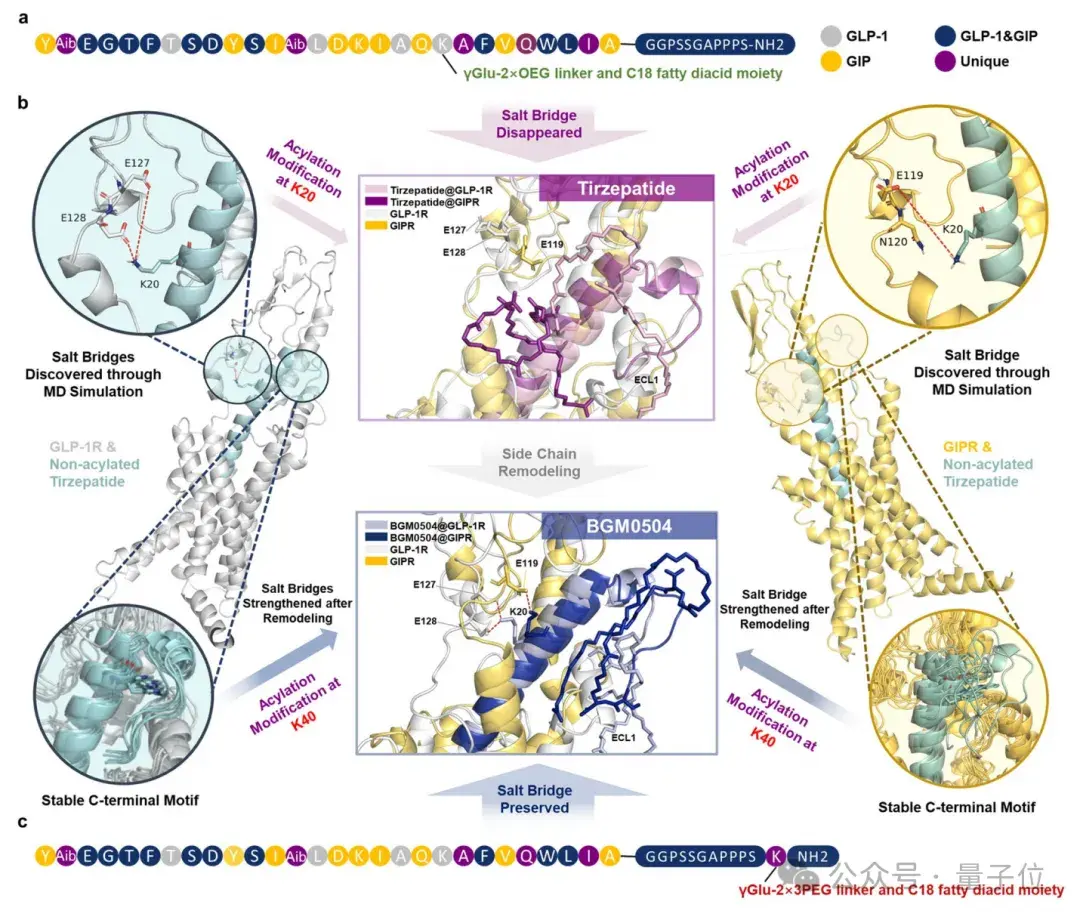
值得关注的是,研究中使用的分子动力学模拟,正是利用了AI算法实现。
在2022年,该团队发布了名为Movable Type的绝对结合自由能算法软件。它配合分子动力学模拟,可以用来提高生物分子自由能计算的准确性和效率。
基于该核心算法而来的数据及算法平台,能够模拟微观世界中疾病靶点的柔性机制和构象变化规律,他们还给该平台起了一个更通俗易懂的名字——分子电影技术。
它基于演绎法技术路线。和常见的统计学路线不同,这种方法不是利用高通量筛选暴力穷举出合适的分子结构。而是基于量子力学、物理模型等,让AI计算推导出相应的结果。
研究团队解释,这就好比天文学,科学家可以通过公式计算出天体运行的复杂变化,模拟轨道运行、捕捉到行星相遇点等。微观世界下,各种分子原子也好比一个个天体,可以借助物理模型计算它们之间的相互作用。
由此带来两方面好处:
第一、相较于传统结构生物学实验方法,这种利用AI的方法能够动态还原分子作用的过程。
X射线衍射、冷冻电镜等实验手段能做到的还只是将生物分子近天然状态下某一时刻的三维结构进行呈现,如果分子的运动柔性比较大,“单帧”的呈现可提供的信息非常有限。
AI解析则能通过模拟的方式,更完整模拟呈现分子构象变化和相互作用的过程,这也是为何该方法的别称为“分子电影技术”。
第二、相较于统计学路线的AI制药方法,这种方法不是仅从海量数据中总结规律,而是让AI更深入理解生物、化学、物理等方面模型,从而可以让生成结果更具可解释性,这更满足生物制药领域对底层机制深入了解的需求。
同时,演绎法的技术路线效率也更高。据介绍,本项研究仅从10个化合物设计方案中就找到了目标。而传统实验方法可能需要数千次的尝试。
整个实验流程大致如下:
先通过分子动力学模拟软件来模拟Tirzepatide与GLP-1R和GIPR的相互作用。基于结果重点分析了K20位点的盐桥形成和乙酰化侧链对靶点激动活性的影响。
然后基于模拟结果设计出BGM0504,该化合物通过改变乙酰化侧链的位置来优化与受体的相互作用。
体外实验部分,对BGM0504进行cAMP积累实验,以评估其对GLP-1R和GIPR的激动剂活性。并使用Bio-Layer Interferometry (BLI)技术测试了BGM0504与人类血清白蛋白(HSA)的结合亲和力。
然后在db/db小鼠(一种二型糖尿病模型)中评估BGM0504的体内药效,包括血糖控制、胰岛素水平、体重和食物摄入等。在STZ + HFD诱导的C57 BL/6小鼠(另一种2型糖尿病和NASH模型)中评估BGM0504对糖尿病和NASH的治疗效果。
进一步在Sprague–Dawley(SD)大鼠和猕猴模型中对BGM0504进行药代动力学评估,包括通过静脉注射和皮下注射给药后的血浆清除率、分布体积、半衰期和生物利用度。
最后再进行组织学评估、生化分析以及数据和统计分析等。
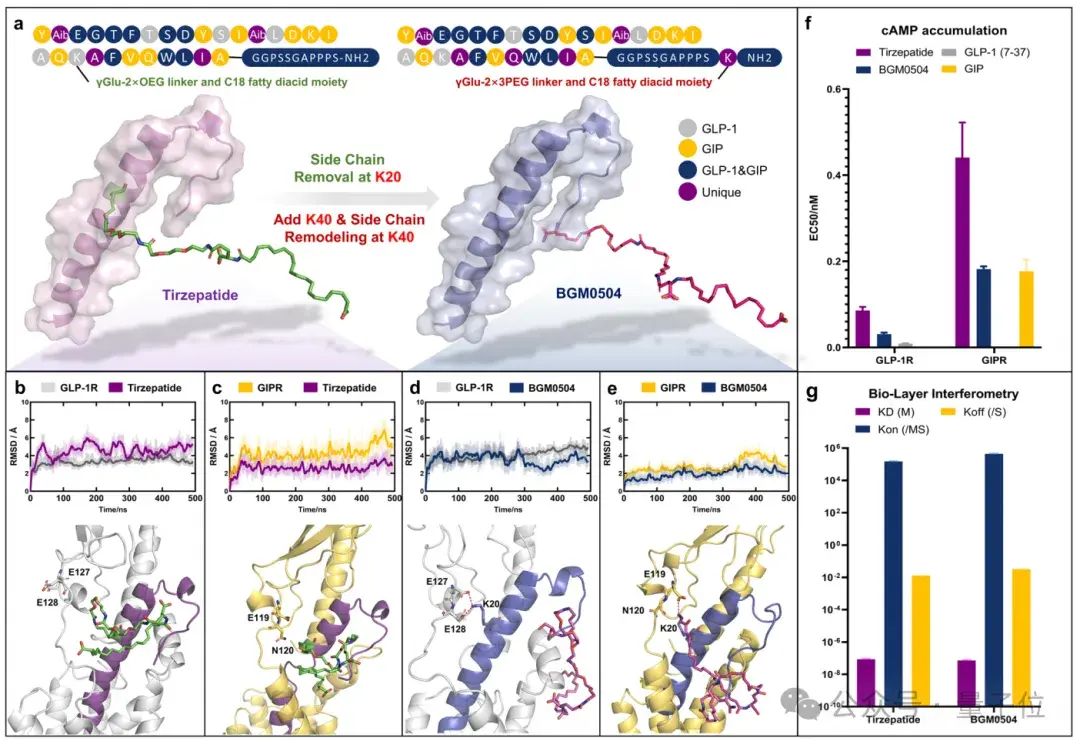
研究表明,在体外实验中,BGM0504在激动GLP-1R/GIPR方面的活性是Tirzepatide的2至3倍,具有更低的EC50值,这表明了其更高的生物活性。
体内药效上,BGM0504显示出比Tirzepatide更好的降低血糖和胰岛素水平的效果,并且能够显著减少体重和食物摄入。
同时在SD大鼠和猕猴模型中的药代动力学研究表明,BGM0504具有延长的半衰期和较高的血浆暴露量,这为其作为长效药物的潜力提供了支持。
因此BGM0504是一个有前景的长效GLP-1R/GIPR双靶点激动剂,在治疗2型糖尿病和肥胖症方面显示出优越的疗效,并且在NASH模型中也表现出改善肝功能和血脂水平的潜力,值得进一步的临床研究和开发。
更值得关注的是,研究中所采用的技术模式,已经在产业中落地应用并取得进展。
据了解,该团队目前已和全球50多家药企达成合作,有2种药物进入到临床三期,3种药物也已开始临床试验。
这些进展背后,都有一个共同的名字:予路乾行。
予路乾行是谁?
予路乾行创立于2021年底,公司总部base苏州,是国内少有的利用分子模拟进行药物开发的初创企业。
创始人郑铮有着深厚的药物开发背景,是AIDD(AI Drug Discovery & Design)领域专家。

他本科就读于北京大学药学系,后赴佛罗里达大学攻读化学博士学位,师从计算化学领域顶级专家、高引学者Kenneth Merz教授。他曾任Quantum Bio药物设计软件公司资深科学家,现在还是武汉理工大学教授、博士生导师。
2021年,郑铮正式回国创业。
当时的生物医药行业正处于快速变化中。全球共有84种新活性物质(NAS)上市,创历史新高。新兴生物制药公司在研产品大约有4700种,占研发总管线的65%。
AI和机器学习在药物设计中的应用也越来越广泛。AlphaFold2宣布开源,成功掀起AI预测蛋白质结构热潮,全球AI制药行业融资总额超220亿美元,其中中国发生49起,共计127亿人民币。
但予路乾行的创立并不仅仅是因为看到了趋势和热度。
郑铮表示,在学生时代就意识到药学行业最终极的意义在于落地应用。
从2000年到现在,生物医药领域有一些标志性的重大事件。其一是薛定谔公司的药物发现完整软件包上市,它极大地推动了计算化学和分子模拟技术的发展,提高了科学研究和药物开发的效率和成功率,让生物医药来到了全新时代。
其二是英伟达推出CUDA,将GPU强大的计算能力引入到科学领域、加速计算机模拟计算,让行业的效率进一步提升。
后面随着AI技术、计算技术不断发展,利用计算机模拟进行药物开发的趋势越来越明显。2020年,主打通过先进计算方法设计药物的薛定谔公司成功上市,成为行业内首家上市的计算药物研发公司。
郑铮在读博期间,深耕分子模拟的力场开发和采样算法研发领域,所开发的GARF力场引入量子力学精度的AI模型,大幅提升了运算精度;所开发的Movable Type自由能算法分别申请了美国和国际专利,并授权给一家美国CADD软件公司进行商业化。在回国创业前,郑铮主导了Movable Type算法软件的开发,该软件在多家大型药企内部的同类软件测试中胜出。这一算法不仅得到了1981年诺贝尔化学奖得主罗德·霍夫曼的认可和推荐,还获得了美国全球药物设计算法挑战赛第二名。
除了郑铮本人外,予路乾行的核心团队均有着深厚的生物制药、化学背景。
首席科学家Kenneth Merz教授是美国密歇根州立大学超算研究中心院长,全球首个解析式物理大模型“Amber力场”的发明人,化学信息学国际顶级期刊 J. Chem. Inf. Model 主编,美国化学协会(ACS)计算机与化学部主席,理论化学、计算生物学领域全球顶级专家。近10年连续被科睿唯安(Clarivate Analytics)评为计算化学与计算生物学领域全球高被引科学家。
首席技术官刘昊博士是美国佛罗里达大学化学博士、厦门大学化学学士;曾于美国基因泰克(Genentech)公司担任数据工程师,负责大数据采集及分析、数据库建立及管理工作。

“科班出身”+“手握核心技术”,这两点构成了予路乾行创立的核心基础。
自创立以来,予路乾行已完成两轮融资,其中数千万元的第二轮融资由复星医药旗下复健苏州基金领投、中新资本跟投。
同时也和国内外多家药企完成合作,积累有四十余条服务/合作研发管线共同推进。其中有近10条管线是完成了“从0到1”的构建。
为什么能走得这么快,予路乾行做对了什么?
AI制药的iPhone时刻已到来
梳理来看,予路乾行关键把握住了三方面:
- 差异化技术路线
- 清晰的商业模式
- 广阔的行业前景
首先,在AIDD赛道上,目前很多企业聚焦在算法开发方面。尤其在国内市场中,选择分子模拟路线的初创企业并不多。
《中国AI制药企业白皮书》中统计,国内30余家布局AI药物靶点发现与验证的初创企业中,仅有予路乾行聚焦在分子模拟技术领域。
这使得予路乾行天生具备更多差异化优势。而且这条路线的可行性,通过薛定谔公司的成功上市即可验证。
更深层面,解析式模型天生具备的更强可解释性,是生物制药领域的刚需。对于任何一家药企而言,制备新型药物的同时,更关键问题在于对背后机制的准确理解。
郑铮解释,就像每个数学公式中的参数都有对应意义,解析式模型是在物理模型基础上建立,它能更好理解“公式”的意义在哪,也能在迁移过程中花费更小的代价找到对应参数。与此同时,它对专业数据的需求也更低。
要知道,缺少药物研发的数据资源已经成为互联网科技大厂、初创企业入局AI制药的难关。而予路乾行从底层技术路线上更大程度规避了这一问题。

其次,予路乾行在2年内快速摸清了商业模式。
通过深度参与Biotech企业的药物开发全流程,予路乾行为大型药企提供高效的AI平台,赋能药物开发早期设计和后期临床等环节,和企业共享管线的未来收益权,这样能以轻资产的形式运营起来,一方面可以积累更多合作案例,另一方面也能换取更大的未来收益。
同时在业务布局上,予路乾行海内外双管齐下。
在新药研发探索上,海外市场非常广阔,中国企业凭借效率上的优势,能更受青睐。郑铮举例说,之前他们和一家美国公司表示1周内就能完成第一份交付,对方直接惊呆了,因为一般的时间周期可能需要1个月。
国内市场上,因为予路乾行建立了一种新的药物研发范式,相较于传统试错方法效率更好,自然也能得到更多关注。

最后在市场前景上,AI制药不可估量。
目前,人类疾病相关的具有临床意义的蛋白靶点中有接近85%的蛋白缺乏明确的结合口袋或配体、或是内源性底物的亲和力过高,且通过传统方法“难以成药”,因此被认为是不可成药靶点。长期以来,靶向蛋白的药物受限于有限的蛋白种类,极大地限制了药物发展。
如今随着AI、计算等技术发展,过去难以计算或难以预测的领域被逐渐攻破,85%不可成药靶点成为了新的蓝海。予路乾行表示,他们正是瞄准这一部分展开创新。
今年,AlphaFold3发布标志着AI预测蛋白迈向全新阶段。不仅限于蛋白质结构,所有生命分子的结构和相互作用,都能以前所未有的精度被预测,人类对生命进程可以有更加充分的理解。
英伟达则掀起了市场方面的风暴。2023年以来,其旗下投资部门NVentures至少投资了12家AI制药企业。
黄仁勋更是表示:
学电脑的时代已经过去了,生命科学才是未来。
他甚至希望,对AI的运用,可以把“药物发现”变成一个工程领域,而不仅仅是生命科学。
聚集到国内,制药领域在过去十年左右快速发展,从原来的只能做仿制药,发展到如今可以fast-follow、研制创新药。这背后有来自国家在政策、人才等方面的持续扶持。
这也是为何予路乾行选择回国创业的一大原因。
对于未来前景,郑铮非常乐观,他认为人们总是低估技术在5-10年中能实现的事情。
我认为现在AI制药已经到了iPhone时刻,业内能明显感知到。再过5年,市场就能充分感知到这种变化。
怎样才能抵达这样的未来?
终日乾乾,与时偕行。
予路乾行从成立第一天起,就想好了。
论文地址:
https://www.nature.com/articles/s41598-024-66998-8
- 业界首创,海螺集团携手华为发布水泥建材人工智能大模型2025-04-23
- 本周三!机器人与数字化转型应用解析,线上研讨会诚邀你来围观2025-04-22
- 数势科技谭李:企业级AI应用不止ChatBI,拿到数据不等于拿到洞见 | 中国AIGC产业峰会2025-04-22
- 3分钟搭建一个调用支付宝的智能体,MCP爆发,蚂蚁推了一把2025-04-18











